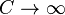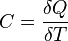Молярную тепловую энергию газов можно рассматривать как сумму энергий отдельных атомов и молекул:
Q= NAε
Где N
A -- число Авогадро, ε – средняя энергия возбуждения одного атома или молекулы.
Переход тепловой энергии в виде излучения через вакуумные перегородки требует рассмотрения в
процессах термодинамики механизмов КМ.
В соответствии с КМ, механизмы приращения тепловой энергии излучения сопровождаются переходами электронов по энергетическим уровням. Следовательно, молярная тепловая энергия газов отдельно взятых элементов прямо пропорциональна средней энергии электронов на возбужденных энергетических уровнях:
Q∝E
где Q – молярная тепловая энергия излучения; E -- средние энергии электронов на возбужденых энергетических уровнях
Это хорошо согласуется с законом сохранения энергии:
Эне́ргия — скалярная физическая величина, являющаяся единой мерой различных форм движения материи и мерой перехода движения материи из одних форм в другие. Введение понятия энергии удобно тем, что в случае, если физическая система является замкнутой, то ее энергия сохраняется во времени. Это утверждение носит название закона сохранения энергии. http://ru.wikipedia.org/wiki/%D0%AD%D0%BD%....%B3%D0%B8%D1%8Зависимость температуры (интенсивности теплового излучения) от давления позволяет предположить, что интенсивность теплового излучения формируется при неупругих ударах атомов. Это хорошо согласуется с МКТ и КМ.
При стремлении давления к нулю, температура тоже стремится к нулю при любых энергиях электронов. Это свидетельствует, что без неупругих ударов электроны на любых энергетических уровнях могут находиться неопределенно долгое время.
Для перехода электрона в верх по энергетическим уровням электрон должен захватить фотон с энергией перехода. В соответствии с механизмами неупругих столкновений, для перехода электрона вниз по энергетическим уровням электрон должен получить импульс торможения. Если энергии удара не достаточно для перехода электрона на более низкий энергетический уровень, то удар будет упругим без тормозного излучения. Если нет излучения, то соответственно нет и температуры.
Например, при увеличении давления увеличиваются мощности ударов атомов и молекул друг с другом. Это сопровождается увеличением интенсивности тормозного излучения (температуры). Квантовое охлаждение сопровождается излучением тормозного излучения и снижением электронов по энергетическим уровням. Переходы электронов между низкими уровнями имеют большую частоту излучения, следовательно, для переходов электронов требуются большие энергии ударов (давления). Это объясняет механизм зависимостей между энергиями электронов (молярной тепловой энергией), давлением и интенсивностью удельного излучения (температурой).
Это хорошо согласуется с определением температуры:
... мерилом температуры является не само движение, а хаотичность этого движения. Хаотичность состояния тела определяет его температурное состояние, и эта идея (которая впервые была разработана Больцманом), что определенное температурное состояние тела вовсе не определяется энергией движения, но хаотичностью этого движения, и является тем новым понятием в описании температурных явлений, которым мы должны пользоваться ... (П. Л. Капица)
http://ru.wikipedia.org/wiki/%D0%A2%D0%B5%...%83%D1%80%D0%B0
Рис. 1. Изотермы -- красные кривые, адиабаты -- черные кривые.
По горизонтальной оси -- объем, по вертикальной оси -- давление.
Является существенным, что в изотермических системах изменение состояний газов сопровождается приращением тепловой энергии. Например, в изотермической системе из двух камер, в которых P1≠P2, соответственно и V1≠V2, молярная тепловая энергия (средние энергии возбуждения электронов) тоже различна Q1≠Q2:
V1P1=V2P2, при T1=T2, Q1≠Q2
Является существенным, что в изотермических
процессах молярный объем зависит от молярной тепловой энергии (средней энергии электронов на возбужденных энергетических уровнях) и давления. Это можно объяснить тем, что каждый атом или молекула имеют определенный объем, определяемый объемом электронных оболочек атомов, а также кулоновскими силами отталкивания между электронными оболочками соседних атомов или молекул и внешним давлением. Кулоновские силы отталкивания между электронными оболочками атомов и молекул объясняют упругость газов, а также зависимость изменения молярного объема газов от давления:
V=f(Q,P)
Где f -- функция зависимости между температурой, давлением и молярной тепловой энергией (средней энергией электронов на возбужденных энергетических уровнях).
Таким образом, можно сделать вывод, что
температура является ВТОРИЧНЫМ фактором от взаимодействий между атомами в зависимости от давления и внутренней тепловой энергии Q (средней энергии электронов на возбужденных энергетических уровнях).
T=f(P,Q)
где f -- функция зависимости температуры от давления и молярной тепловой энергией (средней энергией электронов на возбужденных энергетических уровнях)
В изобарных
процессах, тепловая энергия полностью тратится на работу по изменению объема:
∆Q=A=P∆V, при P=constant,
Где A -- работа
В соответствии с КМ, изменение объемов при приращении тепловой энергии можно объяснить тем, что приращение тепловой энергии излучения сопровождается переходом электронов по энергетическим уровням, что сопровождается изменением объемов электронных оболочек атомов и молекул. Следовательно, можно сделать вывод, что в изобарных
процессах приращение тепловой энергии прямо пропорционально приращению молярного объема:
Q∝PV, при P=constant. (4)
В
адиабатических процессах, зависимость температуры от давлений, а так же стремление температуры к нулю при стремлении давления к нулю, при любых средних энергиях возбужденных электронов в атомах, свидетельствует, что:
1. электроны на возбужденных энергетических уровнях могут находиться неопределенно долгое время;
2. температура (интенсивность теплового излучения) определяется интенсивностью неупругих ударов атомов и молекул.
В
адиабатических процессах, газы имеющие разные молярные тепловые энергии (средние энергии электронов на возбужденных энергетических уровнях) имеют разные адиабаты:
Как видно из Рис.1., адиабаты зависят от молярной тепловой энергии в газах, что можно записать как:
PVγ=constant=f(Q)
или
PVγ=f(Q), при Q=constant, (5)
Где f – функция зависимости constant от молярной тепловой энергии (средней энергии электронов на возбужденных энергетических уровнях).
В
адиабатических процессах,
по изменениям konstant, в соответствии с изменениями молярной тепловой энергии Q, можно определить функцию зависимости изменения constant в соответствии с изменениями молярной тепловой энергии constant =f(Q).