Результаты моделирования разделим на шесть серий.
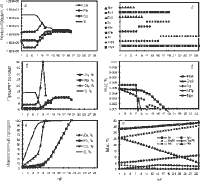 |
| Рис.6.2. Базовая модель мобилизации IS-2 |
1. Базовая
модель выщелачивания (IS-2) - название "базовая" чисто условное
и определяется тем, что при параметрах данной модели выполнено максимальное
количество расчетов.
Условия и параметры моделирования:
T=370oС; P=1 кбар (приблизительно отвечает литостатическому давлению);
масса гранита в реакторе равна 10 кг (гранит Холста), т.е. начальное отношение
порода/вода соответствует 10 (R/W=10; количество воды в единичной порции (волне)
первичного раствора равно 1 кг; солевой состав этого раствора: H2CO3=0.5 m; NaCl=1.0
m; HCl=0.1 m, где m - моляльная концентрация (моль/1000 г H2O); через реактор последовательно проходит 30
порций (при необходимости до 100) или волн первичного раствора, поэтому интегральное
отношение порода/вода изменяется до 0.33 или lg(R/W) = -0.5.
В
таблице 6.2 (данные для 1, 10, 20 и 30 волн) и на рисунке 6.2 приведены
результаты расчетов для двух продуктов реакции: раствора выщелачивания (рис.6.2а-в)
и изменяющейся породы (рис.6.2г-е)18. На всех графиках рисунка
6.2 по оси абсцисс отложены последовательные порции или волны (NF) первичного
раствора.
Уже на первой волне взаимодействия
формируются основные характеристики раствора выщелачивания (см. табл.6.2). В растворе появляются K (0.2 m), Ca (0.0098
m), Mg (1.9.10-5
m), Al (4.2.10-5
m), Si (0.0223 m), Fe (0.0045 m). Устанавливается близ нейтральное значение
pH (5.324), уменьшается концентрация Na (от 1 m до 0.88 m). Концентрации рудных
компонентов имеют достаточно высокие значения: Zn - 1.81.10-4 m, Pb - 1.68.10-5
m, Cu - 1.27.10-5 m, S - 2.16.10-3 m.
По мере вступления в
реакцию всё новых порций первичного раствора в системе происходят изменения,
которые сопровождаются последовательным возрастанием концентраций рудных элементов
в растворе выщелачивания: для Zn в 11 раз, от 1.8.10-4m в первой волне до 2.10-3m в девятой; для Pb в 12 раз, от 1.7.10-5m в первой волне до 2.10-4 m в 13-19 волнах; для Cu в 22 раза, от 1.3.10-5
m в первой волне до 2.9.10-4
m в 13-19 волнах (концентрация Cu увеличиваются в 120 раз при сравнении 2-6
волн и 13-19) (рис.6.2а). Одновременно с ростом
концентраций рудных компонентов происходит уменьшение равновесной концентрации
сульфидной серы от 2.2.10-3 в первой волне до 3.4.10-4 m в 19-ой, т.е. в 65 раз.
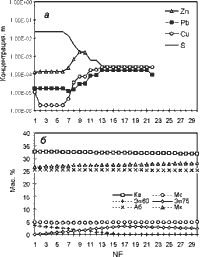 |
| Рис. 6.3. Модель мобилизации IS-23 |
Как видно из рисунка
6.2а-в, выщелачивание компонентов происходит неравномерно по волнам.
Так, на первых 6 волнах Zn в раствор переходит практически равномерно - по 4%
от всего металла, содержащегося в граните, а суммарный его выход в раствор составляет
23.7% (см. рис.6.2б, в).
После шестой волны интенсивность мобилизации цинка резко возрастает и составляет
6 % на NF=7; 19% на NF=8; 40% на NF=9; на десятой волне цинк выщелачивается
полностью, и процент его перехода в раствор уже не отвечает потенциальной мобилизующей
способности первичного раствора (12% на NF=10 - это весь остаток цинка в породе).
Выщелачивание Pb и Cu
происходит менее интенсивно, но имеет аналогичную тенденцию: низкий процент
перехода в равновесный раствор на первых шести волнах (Pb по ~0.9%, Cu по ~0.1%),
а затем начинаются изменения и рост. На рисунке 6.2б,
в видно, что если на первых 10 волнах взаимодействия
вынос Pb опережал вынос Cu (12.56% Pb и 10.65% Cu - суммарный процент выноса
при изменении NF от 1 до 10), то позже они выравниваются, и полное выщелачивание
этих металлов и сульфидной серы происходит одновременно на двадцатой волне.
При этом концентрация сульфидной серы в равновесном растворе становится меньше,
чем суммарная концентрация Pb и Cu (на NF=19 -1.98.10-4
m Pb; 2.88.10-4 m Cu и 3.42.10-4 m S). Содержание сульфидной серы превышает концентрации
всех рудных металлов только на NF = 1-13.
Кислотность раствора выщелачивания (pH=5.3), ионная сила (0.7)
и макросостав (K - 0.2; Na - 0.88; Ca - 0.005-0.007; Si - 0.02; Fe - 0.004;
Cl - 1.1; C - 0.5 m) остаются практически постоянными на всех NF (см. табл.6.2).
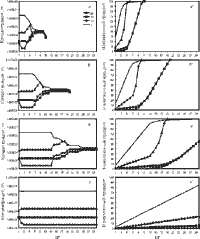 |
| Рис. 6.4. Зависимость характера мобилизации рудных компонентов от массы
породы в реакторе (модель IS-2, гранит месторождения Холст) |
Главная причина изменения
концентраций металлов в растворе выщелачивания - постепенный вынос сульфидной
серы из породы. Пока её количества достаточно для поддержания концентраций в
равновесии с сульфидами, концентрации рудных элементов в растворе не изменяются.
Следствием выноса серы является изменение равновесной ассоциации рудных минералов
в изменяющемся граните (см. рис.6.2г, д).
При выщелачивании первым из сульфидов исчезает пирротин - после прохождения
через реактор 6 порций раствора. Пока он есть, роста растворимости рудных сульфидов
не происходит. Это выражается платообразными участками на кривых изменения концентраций
Zn, Pb, Cu (см. рис.6.2а). Минимум на кривой выщелачивания Pb (NF=7)
связан со сменой гидросульфидных комплексов свинца на хлоридные, которые являются
преобладающими для Zn и Cu во всем диапазоне концентраций серы. Резкое уменьшение
концентрации меди (на 2-6 волнах) совпадает с изменением в равновесной ассоциации
фаз: появление менее железистого эпидота (см. рис.6.2г). Уменьшение количества
сульфидной серы в системе отчетливо отражается в последовательной смене устойчивых
сульфидов меди (см. рис.6.2г, д): халькопирит на 1-7 волнах, борнит на
8-12, халькозин на 11-19, а также в быстром росте содержаний Cu в растворах,
равновесных с ними (к 7 волне из породы вынесено 93% S и только 1% Cu).
Макросостав породы после
реакции с 30 порциями исследуемого первичного раствора изменяется (см. табл.6.2.
и рис.6.2е) следующим образом. Происходит увеличение содержаний кварца
(от 33 до 38 масс.%), альбита (от 26 до 36%), мусковита или серицита (от 5 до
11%); уменьшение содержаний калиевого полевого шпата (от 26 до 5%) и эпидота;
практически не меняется содержание железисто-магнезиального хлорита (5.6-5.9%)
и актинолита (1.1-1.2%). Главные из происходящих перемен очевидны. Поскольку
первичный раствор данной модели содержит 1 m NaCl и 0.1 m HCl, то при его взаимодействии
с калиевым полевым шпатом происходит образование альбита, мусковита и кварца
(4Мк+Na+(р-р)+2H+(р-р) =
Мс+Аб+6Кв+3K+(р-р)). На рисунке 6.3 представлены
результаты расчетов по модели IS-23, где все параметры , кроме состава первичного
раствора (H2CO3=0.5; NaCl=0.8; KCl=0.2 m), аналогичны базовой
модели. При этом pH растворов выщелачивания остается таким же, как в модели
IS-2, но растворы имеют более низкую ионную силу: 0.6 против 0.7 в модели IS-2,
за счет исключения из состава первичного раствора 0.1 m HCl. Введение 0.2 m
KCl приводит к практическому постоянству состава породы после прохождения через
нее 30 порций раствора (кварц 31.9-32.6%, альбит 25.2-25.2%, микроклин 26.6-28.1%,
мусковит 4.63-4.96%). Сравнение рисунков 6.2 а и 6.3а, а также
6.2е и 6.3б, показывает, что такое заметное изменение состава
породы не оказывает принципиального влияния на выщелачивание рудных элементов.
2. Зависимость
характера мобилизации рудных компонентов от массы породы в реакторе. Все
условия соответствуют базовой модели (IS-2), кроме исходной массы гранита месторождения
Холст в реакторе. На рисунке 6.4 представлена часть результатов расчетов для
5, 10, 20 и 50 кг породы.
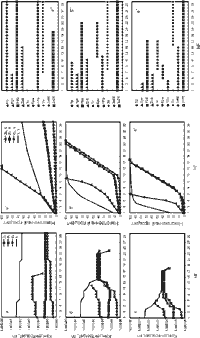 |
| Рис. 6.5. Зависимость характера мобилизации рудных компонентов от количества
сульфидной серы в граните месторождения В. Згид |
Происходит пропорциональное
изменение характеристик растворов выщелачивания. Сравнение результатов удобно
проводить с рисунками 6.4б и б', поскольку они являются фрагментом
данных по базовой модели, где масса гранита составляет 10 кг (см. рис.6.2а,
в). Уменьшение массы гранита в 2 раза (до 5 кг) приводит к укорачиванию
в 2 раза платообразного интервала равных концентраций при низких значениях NF
и, соответственно, к аналогичному уменьшению области устойчивости пирротина.
Увеличение - в 2 и 5 раз (до 20 и 50 кг) выражено в удлинении этого плато практически
в 2 и 5 раз (до NF=13 и NF=32, соответственно). В пропорционально смещенных
точках концентрации растворов полностью идентичны.
Такие же смещения можно видеть на графиках правой части рисунка
6.4. Например, выход на близкий процент суммарного выщелачивания цинка из породы
происходит: а' - 23.83% на NF=3; б' - 23.67% на NF=6; в' - 23.62% на NF=12;
г' - 23.70% на NF=30.
При прохождении 30 порций
первичного раствора через реактор с 50 кг гранита ассоциация минералов с пирротином
устойчива, и не достигается суммарный состав системы, способствующий резкому
возрастанию концентраций металлов в равновесном растворе. Естественно, что дальнейшее
взаимодействие приводит к эффектам, установленным для меньших количеств породы
(полное выщелачивание металлов происходит на 96-ой волне).
3. Зависимость
характера мобилизации рудных компонентов от состава породы в реакторе. Сохранены
условия базовой модели, но расчеты и сопоставления результатов сделаны для гранита
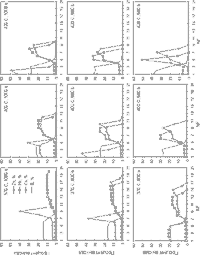
Холста и В. Згида (составы в табл.6.1). На рисунке
6.5 приведены результаты расчетов для гранита месторождения В. Згид. Сопоставление
проводим с данными для гранита месторождения Холст (см. рис.6.2).
Сравнение рисунков 6.2а,
в, г и 6.5а,
a', a'' показывает,
что характер мобилизации рудных компонентов из этих пород при одинаковых условиях
различен. При взаимодействии первичного раствора с гранитами В. Згида (см.
рис.6.5а) не происходит быстрого роста концентраций Zn, Pb и Cu. Вынос
Zn опережает вынос S (100% Zn и только 45% S на NF=16), концентрация сульфидной
серы снижается только в 4 раза после прохождения 30 порций раствора, а суммарный
вынос Pb и Cu составляет только 23 и 5% от исходных содержаний в породе, соответственно.
Естественно предположить, что различия обусловлены разницей в химических составах
гранитов Холста и В. Згида. Данные таблицы 6.3
свидетельствуют, что состав измененных пород практически одинаков. Тем не менее,
имеются небольшие, но важные отличия по малым минералам, появление которых служит
индикатором различий в условиях выщелачивания. К главным из них относится присутствие
пирита в равновесной ассоциации минералов, образующейся при реакции первичного
раствора с гранитом В. Згида (см. рис.6.5а'' и табл.6.3).
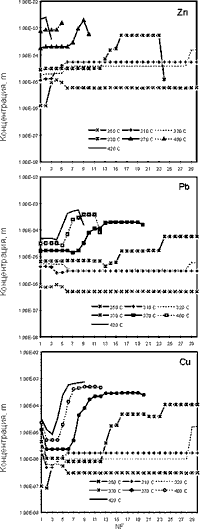 |
| Рис. 6.6. Зависимость характера мобилизации рудных компонентов от температуры
Прочие условия соответствуют модели IS-2 |
Наличие пирита указывает,
что гранит В. Згида имеет избыточное количество сульфидной серы по сравнению
с гранитом Холста. Действительно, если посчитать отношение FeS/(FeS+FeO), то в граните В. Згида
оно составит 12.44 мол.%, а в граните Холста - 2.51 мол.%. Данные Готмана Я.Д.
и Малаховой В.М. [1966], (см.
табл.6.1), показывают, что осреднение анализов для гранитов В. Згида
проводилось по результатам опробования вблизи и вдали от жильных тел, а во всех
анализах проб вблизи жил содержание сульфидной серы выше 0.15 мас.% (до 0.5%).
Вдали же от жил содержания сульфидной серы приближаются к данным по гранитам
Холста, т.е. ~0.05-0.07 мас.%.
"Избыточность"
серы в гранитах В. Згида мы проверили, выполнив дополнительные расчеты,
в которых изменили соотношение FeS/(FeS+FeO) в граните, т.е. уменьшили
количество сульфидной серы и увеличили содержание оксидного железа (при этом
сумма железа не меняется). Эти данные представлены на рисунке
6.5б, в,
где FeS/(FeS+FeO) составляет 4.61% и 2.3%. Сопоставление рисунков
6.5в (в', в'') и 6.2а (в, г) показывает,
что уменьшение сульфидной серы изменяет характер мобилизации рудных компонентов
из гранита В. Згида и приводит его к виду, практически полностью аналогичному
выщелачиванию из гранитов Холста. Конечно, и здесь остаются отличия. Так, из-за
меньшего содержания железа в гранитах В. Згида пирротин устойчив только
при NF от 1 до 3. Но общая тенденция мобилизации компонентов имеет характерный
вид, отмеченный для базовой модели.
4. Влияние
температуры на характер мобилизации рудных компонентов. Все параметры, кроме
температуры, аналогичны модели IS-2. Расчеты проведены при температурах от 250
до 420oС. Частично результаты для рудных элементов представлены на
рисунке 6.6. Главным следствием падения температуры в реакторе является уменьшение
растворимости сульфидов рудных элементов, присутствовавших в граните,
из-за чего картина выщелачивания изменяется. Так, для первой порции раствора
(NF=1) при температурах 420 и 250oС имеем, соответственно,
для Zn 2.15.10-3 и 1.26.10-6
m (различие в 1700 раз), для Pb 4.82.10-5 и 7.68.10-7 m (различие в 60
раз), для Cu 3.03.10-5
и 9.45.10-8
m (различие в 320 раз), для S 4.35.10-3 и 2.65.10-3
m (различие в 15 раз).
Сравнение характера выщелачивания
при разных температурах можно сделать по графикам рисунка
6.6 (кривые при 370oС отвечают базовой модели). Увеличение температуры
до 400 и 420oС приводит к сокращению числа порций первичного раствора,
при которых рудные сульфиды сохраняются в породе. Так, при 400oС
сфалерит устойчив до NF=4, а галенит и сульфиды меди до NF=11. При 420oС
сфалерит устойчив до NF=2, а галенит и сульфиды меди до NF=8. Уменьшение температуры
сдвигает границу устойчивости сульфидов в сторону роста NF. Например, для Zn:
370oС - 9; 360oС - 11; 350oС - 14; 340oС
- 18; 330oС - 23; 320oС - 41; 310oС - 57; 300oС
- 70; 280oС - 86; и при 250oС - более 100. Для Pb и
Cu смещения происходят аналогично, но NF на 10-20 единиц больше. Соответственно,
при понижении температуры сдвигаются по NF и "платообразные" участки
максимальных концентраций металлов (при температуре ниже 330oС эти участки
при NF от 1 до 30 не проявляются).
Имеются определенные различия в равновесных минеральных ассоциациях.
При температурах 360-420oС равновесная ассоциация соответствует базовой
модели (отличия только по NF). При температурах 340-350oС появляется
пирит (при NF от 2 до 8-10). При температурах 250-330oС к равновесной
ассоциации минералов добавляется кальцит (в количестве 0.1-1.6 мас.%).
 |
| Рис. 6.7. Влияние давления на мобилизацию рудных компонентов |
5. Влияние
давления на характер мобилизации рудных компонентов. Расчеты проведены при
температурах 370, 400, 420oС и давлениях 400, 600, 800, 1000 бар
для первичного раствора и породы, соответствующих базовой модели. Сравнение
результатов расчетов представлено на рисунке 6.7 (графики процента выхода компонента при данном
NF от суммарного мольного количества элемента в исходной породе).
При каждой температуре понижение давления приводит к следующим
эффектам:
- росту концентраций металлов в растворе;
- уменьшению NF, при которых металл полностью выщелачивается;
- разделению по волнам максимумов перехода в раствор рудных
элементов.
Рост концентраций при
уменьшении давления от 1000 до 600 бар меньше, чем при увеличении температуры
от 370 до 420oС. Так, при таком росте температуры при P = 1000 бар
концентрации увеличиваются следующим образом (для первой волны): Zn - от 1.81.10-4до 2.15.10-3 m или от 3.6% до 43% выхода (рост в 12 раз),
Pb - от 1.68.10-5
до 4.82.10-5
m или от 0.8% до 2.4% выхода (рост в ~3 раза), Cu - от 1.27.10-5 до 3.03.10-5 m или от 0.4% до 1.0% выхода (рост в 2.4 раза).
Если рассматривать данные по выщелачиванию при постоянной температуре и уменьшении
давления (от 1000 до 600 бар), то для 370oС получим (для первой волны):
Zn - от 3.6% до 18.6% выхода (рост в ~5 раз), Pb - от 0.8% до 1.3% выхода (рост
в 0.6 раза), Cu практически не изменяется. Для 420oС: Zn - от 42.9%
до 100% выхода, Pb - от 2.4% до 6.6% выхода, Cu - даже немного уменьшается на
первых волнах, но потом увеличивается.
Из графиков рисунка 6.7 видно, что уменьшение давления способствует
разделению максимумов выщелачивания металлов, и ряд относительной подвижности
их принимает вид Zn>Pb>Cu. Так, при 1000 бар максимумы выщелачивания Pb
и Cu практически совпадают, и металлы полностью извлекаются из породы одновременно
(при одном NF). При 600 бар: 370oС - Pb имеет максимум на NF=13,
а Cu на NF=15; 400oС - Pb на NF=7,
а Cu на NF=9; 420oС - Pb на NF=5, а Cu на NF=7.
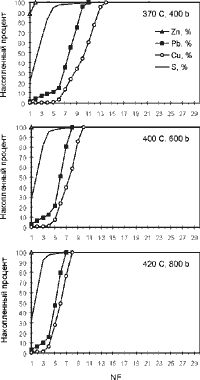 |
| Рис. 6.8. Сравнение моделей мобилизации при разных T и P |
Наряду со смещением максимумов происходит и рост процента выхода
металла в раствор. Так при 600 бар и 370oС к моменту полного выщелачивания
свинца в породе еще остается до 22% меди (при 400 бар - до 40% Cu), при 400oС
- до 42% меди, при 420oС - до 45% меди. Эти соотношения можно видеть
на рисунке 6.8, где приводятся данные о накопленном проценте выхода металлов
при росте температуры и падении давления.
Равновесные ассоциации минералов при уменьшении давления изменяются
в соответствии с ростом растворимости, но в целом остаются эквивалентными базовой
модели. Исключения составляют появление пирита при 370oС и давлениях
400-600 бар (NF от 2 до 5) и магнетита при 420oС и давлении 600 бар
(NF=23 и выше).
6. Влияние
состава первичного раствора на характер мобилизации рудных компонентов. Расчеты
проведены при 370oС и 1 кбар для 17 различных составов первичного
раствора, представленных в таблице 6.4. Изменялись следующие компоненты раствора:
H2CO3 от 0 до 0.5 m; NaHCO3 от 0 до 0.7 m; NaCl от 0.4 до 1.0 m; CaCl2 от 0 до 0.3 m. В единичных моделях задавались
HCl=0.1 m (базовая модель IS-2) и H2S=0.001 m (модель IS-3). Во всех моделях, кроме
базовой, сумма хлора в системе равна 1 m.
Результаты сильно различаются, поскольку заметно меняются составы
систем. Рассмотрение удобнее провести по отдельным группам, в пределах которых
составы первичных растворов изменяются закономерно.
Группа 1. В этой
серии меняется одновременно содержания нескольких компонентов: с ростом CaCl2от 0.05 до 0.3 m, уменьшается H2CO3и увеличивается
NaHCO3(при сохранении
постоянной 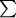 C=0.5 m); NaCl уменьшается от 0.8 до 0.4
m (для поддержания C=0.5 m); NaCl уменьшается от 0.8 до 0.4
m (для поддержания 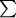 Cl=1.0 m). Cl=1.0 m).
Общая картина последовательности
выщелачивания похожа на базовую модель (сравнение рис.6.2а и 6.9а, б). Однако привнос
в систему компонентов, отсутствовавших в базовой модели (CaCl2и
NaHCO3), приводит к
изменению равновесных минеральных ассоциаций и росту pH (при NF=29-30 в модели
IS-11 pH=5.8, а в модели IS-13 pH=6.0). Происходит частичное уменьшение растворимости
сульфидов меди и свинца (хорошо заметно на уровне NF>15). Это уменьшение
растворимости не одинаково для Pb и Cu. В базовой модели сульфиды Pb и Cu полностью
растворяются одновременно на NF=19. В модели IS-11 минералы меди исчезают на NF=22, а галенит
на NF=23. Дальнейшее изменение составов растворов в этой группе приводит к еще
большему разделению этих металлов: в модели IS-13 (рис.6.9б) для Cu и
Pb имеем соответственно NF=24 и 28.
Изменение составов первичных
растворов вызывает появление минералов, которые не образовывались при условиях
базовой модели. Например, на завершающей стадии выщелачивания в модели IS-13
(и IS-6, см. табл.6.4) образуется кальцит (на NF=25-29).
Рост концентрации кальция в растворе и большая щелочность приводят к увеличению
содержаний кальциевых силикатов: актинолита, эпидота. А это, в свою очередь,
изменяет хлориты: появляется железистый хлорит, и уменьшается (по NF) область
устойчивости железо-магнезиального хлорита. В отличие
от базовой модели, мусковит устойчив только до
NF=14-16, содержание альбита и микроклина значительно выше (например, в модели
IS-13 после прохождения 30 волн первичного раствора имеем 40 мас.% альбита и
15 % микроклина).
 |
| Рис. 6.9. Влияние состава первичного раствора на характер мобилизации
рудных компонентов (370oС, 1 кбар) |
Группа 2. В этой
серии постоянны концентрации CaCl2=0.1 m и NaCl=0.8 m. При постоянном содержании
H2CO3 (кроме модели IS-12) растет NaHCO3: отношение H2CO3/NaHCO3 изменяется
от 1.5 в модели IS-10 до 0.5 в модели IS-20 ( Na увеличивается
от 1.0 до 1.4 m и Na увеличивается
от 1.0 до 1.4 m и  C от 0.5 до 0.9 m, см.табл. 6.4). C от 0.5 до 0.9 m, см.табл. 6.4).
Если первая модель этой группы (IS-10, см. рис.6.9в) близка по результатам к базовой модели,
то конечные модели существенно отличаются (например, IS-19 на рис.6.9г).
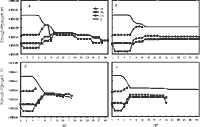
Для этой группы моделей характерны следующие особенности:
- сильное увеличение pH растворов выщелачивания - до pH=7.7-7.8
на NF=30 (например в модели IS-19);
- появление в равновесных
растворах сульфатной серы в преобладающих над сульфидной серой количествах (при
H2CO3/NaHCO3=3/5 в модели IS-19 с NF=25 и далее, при H2CO3/NaHCO3=3/6 с NF=21);
- значительное уменьшение растворимости рудных сульфидов.
Для равновесной ассоциации твердых фаз можно отметить:
- образование магнетита (в модели IS-17 начиная с NF=25, а
в моделях IS-19 с NF=12 и IS-20 с NF=9);
- образование кальцита при меньших степенях взаимодействия,
чем в группе 1 (в IS-19 на NF=10 и выше);
- очень большое содержание альбита - на NF=30 в моделях от
IS-17 до IS-20 имеем соответственно 48.3; 54.9; 57.7 и 58.3 мас.%;
- устойчивость хлоритов и эпидота постепенно уменьшается (так,
в модели IS-19 они имеются только до NF=23).
Такая реакция системы
на изменение составов первичных растворов приводит к сильному уменьшению суммарного
процента выщелачивания рудных элементов за 30 этапов взаимодействия. Так, в
модели IS-19: Zn выщелачивается полностью при NF=22, а Pb, Cu и S к NF=30 извлеклись
из гранита соответственно на 16.7%, 41.4% и 98.4%. Еще сильнее степень выщелачивания
уменьшается в модели IS-20: при NF=30 имеем для Zn, Pb, Cu и S соответственно
43.6%, 7.3%, 16.8% и 96.7%. Следовательно увеличение концентрации NaHCO3 в первичном растворе вызывает изменение последовательности
выщелачивания от Zn>>Pb=Cu к Zn>Cu>Pb.
 |
| Рис. 6.10. Изменение характера мобилизации в системах с различными первичными
растворами при падении давления или росте температуры |
Группа 3. При
постоянных концентрациях CaCl2 и NaCl (0.2 и 0.6 m) увеличивается содержание
NaHCO3 (от 0.3 до 0.7
m) при отсутствии H2CO3 (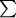 Na Na 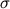 величивается
от 0.9 до 1.3 m и величивается
от 0.9 до 1.3 m и 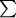 C от 0.3 до 0.7 m, см. табл.6.4).
Результаты расчетов для двух растворов приведены на рисунке 6.9д, е. C от 0.3 до 0.7 m, см. табл.6.4).
Результаты расчетов для двух растворов приведены на рисунке 6.9д, е.
В целом, тенденция выщелачивания близка к описанной для растворов
группы 2. Однако имеются и существенные отличия. К наиболее важным из них можно
отнести:
- преобладание сульфатной серы над сульфидной на более ранних
этапах взаимодействия (в модели IS-9 с NF=19 и далее);
- резкий скачок в растворимости сульфидов на завершающих этапах
выщелачивания при переходе системы в окисленное состояние, которое характеризуется
появлением гематита в равновесной ассоциации минералов (гематит образуется в
моделях IS-7, IS-8 и IS-9);
- появление кальцита и магнетита относительно раньше, если
проводить сопоставление результатов для моделей с равными 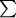 C
(например, IS-18, где кальцит образуется начиная с NF=14, и IS-9, где кальцит
устойчив с NF=8), причем количество кальцита на NF=30 может достигать 6 мас.%. C
(например, IS-18, где кальцит образуется начиная с NF=14, и IS-9, где кальцит
устойчив с NF=8), причем количество кальцита на NF=30 может достигать 6 мас.%.
Эти особенности приводят
к необычному виду кривых мобилизации (см. рис.6.9е). Очевидно, что если бы отсутствовал скачок растворимости
сульфидов при образовании гематита, то последовательность выщелачивания металлов
осталась бы Zn>Cu>Pb. Однако этот эффект приводит к порядку мобилизации,
близкому к базовой модели: Zn>Pb>Cu (например, в IS-9 имеем для Zn, Pb
и Cu соответственно NF=19, 21 и 23).
 |
| Рис. 6.11. Характер мобилизации компонентов при уменьшении концентрации
первичного раствора базовой модели в два раза |
Необходимо отметить,
что внешние условия (температура и давление) могут принципиально изменить картину
выщелачивания. На рисунке 6.10 приведены два примера такого влияния. Модель
IS-12 (группа 2 из табл.6.4 и рис. 6.10а, б) дает сложный характер мобилизации при
P=1000 бар, но уменьшение давления до 600 бар превращает ее практически в аналог
базовой модели (при этом изменяется и порядок мобилизации с Zn>Cu>Pb на
Zn>Pb>Cu). Модель IS-3 (рис. 6.10в, г;
состав раствора H2CO3=0.5 m; NaCl=1 m; H2S=0.001
m) дает очень растянутую по NF мобилизацию Pb и Cu при 370oС, но
резко сокращает ее при 400oС.
В группах 1-3 рассматривались
первичные растворы с  Cl=1 m, но общая концентрация
была иногда существенно более единицы. Для сравнения приведем данные по реакции
с раствором, концентрация которого в два раза ниже концентраций в первичном
растворе базовой модели (модель IS-24, рис. 6.11). Двукратное уменьшение суммарного
хлора (до 0.55 m) приводит к сильному падению растворимости
сульфидов по сравнению с моделью IS-2. Для NF=1 имеем: Zn 2.36.10-5 против 1.81.10-4
m (уменьшение в 7.7 раз), Pb 1.48.10-5 против 1.68.10-5 m (уменьшение в 1.1 раза), Cu 5.79.10-6 против 1.27.10-5 m (уменьшение в 2.2 раза). Изменение растворимости
сульфидов приводит к увеличению интервалов полного выщелачивания: Zn до NF=17,
Pb до NF=41, Cu до NF=44, т.е. вместо Zn>>Pb=Cu для базовой модели получаем
в IS-24: Zn>>Pb>Cu. Cl=1 m, но общая концентрация
была иногда существенно более единицы. Для сравнения приведем данные по реакции
с раствором, концентрация которого в два раза ниже концентраций в первичном
растворе базовой модели (модель IS-24, рис. 6.11). Двукратное уменьшение суммарного
хлора (до 0.55 m) приводит к сильному падению растворимости
сульфидов по сравнению с моделью IS-2. Для NF=1 имеем: Zn 2.36.10-5 против 1.81.10-4
m (уменьшение в 7.7 раз), Pb 1.48.10-5 против 1.68.10-5 m (уменьшение в 1.1 раза), Cu 5.79.10-6 против 1.27.10-5 m (уменьшение в 2.2 раза). Изменение растворимости
сульфидов приводит к увеличению интервалов полного выщелачивания: Zn до NF=17,
Pb до NF=41, Cu до NF=44, т.е. вместо Zn>>Pb=Cu для базовой модели получаем
в IS-24: Zn>>Pb>Cu.
18 На рисунке 6.2, далее в тексте и в таблицах
приняты условные обозначения: Прт - пирротин (FeS), PbS - галенит, ZnS - сфалерит,
Хз - халькозин (Cu2S), Брн - борнит (Cu5FeS4),
ХПр - халькопирит (CuFeS2), Эп - эпидот (Ca2FeAl2Si3O13H),
Эп60 - эпидот Ca2Fe0.6Al2.4Si3013H,
Эп75 - эпидот Ca2Fe0.75Al2.25Si3013H,
Aкт - актинолит Ca2FeMg4Si8O24H2,
Хл75 - хлорит Mg1.25Fe3Al3.5Si2.25O18H8,
Хл50 - хлорит Mg2.5Fe2Al3Si2.5O18H8,
Кв - кварц (SiO2), Мс - мусковит или серицит (KAl3Si3O12H2),
Аб - альбит (NaAlSi3O8), Мк - микроклин (KAlSi3O8)
|

