|
А.В. Амелин, А.А. Скоромец, Л.А. Коренко, Б.Ч. Тумелевич, М.А. Гончар
Кафедра неврологии и нейрохирургии Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова
В начало...
Лечение мигрени в межприступном периоде проводится с целью уменьшения частоты и тяжести атак. Наиболее эффективными препаратами при этом являются бета-блокаторы и антидепрессанты. В простом слепом исследовании проведена сравнительная оценка эффективности амитриптилина (ингибитор обратного захвата серотонина и норадреналина, антагонист 5-
НТ 2-рецепторов) в суточной дозе 12,5-25 мг, флуоксетина (селективный ингибитор
обратного захвата серотонина) в суточной дозе 10-20 мг и мапротилина (селективный ингибитор обратного захвата норадреналина) в суточной дозе 10-25 мг. Длительность лечения мигрени в межприступном периоде составила 12 нед. Каждая группа включала 20 пациентов. Закончили полный курс лечения 46 пациентов: 14 принимавших амитриптилин, 16 - флуоксетин и 16 - мапротилин. Положительные результаты лечения (уменьшение частоты приступов мигрени на 50% по сравнению с исходной) получены у 71% пациентов, принимавших амитриптилин, у 56% принимавших флуоксетин и у 38% принимавших мапротилин. Изученные препараты уменьшали интенсивность и продолжительность приступа головной боли. Индекс качества жизни после лечения повысился в группах пациентов, принимавших амитриптилин и флуоксетин, но не мапротилин. Полученные результаты согласуются с представлением о высокой эффективности антидепрессантов при лечении мигрени в межприступном периоде. Амитриптилин и флуоксетин оказались эффективнее мапротилина. Это косвенное свидетельство того, что эффективность антидепрессантов при мигрени обусловлена ингибированием обратного захвата серотонина и антагонизмом к 5-НТ 2-рецепторам, а влияние на обратный захват норадреналина не имеет определяющего значения.
Фармакотерапия мигрени может быть направлена на купирование приступа мигрени и на лечение болезни в межприступном периоде (профилактика), показанием к которому служит высокая частота (не менее 3 в месяц) и выраженная тяжесть приступов [12]. Целью профилактики является снижение частоты и тяжести мигренозных атак, уменьшение количества употребляемых болеутоляющих средств и повышение качества жизни пациентов.
Среди препаратов, используемых для профилактического лечения мигрени, антидепрессанты относятся к средствам первого выбора благодаря высокой эффективности [1, 2, 11, 14]. Большинство их фармакологических эффектов обусловлено влиянием на обмен серотонина, норадреналина и дофамина. Однако механизм их действия при мигрени неясен. Известно, что эффективность антидепрессантов при мигрени не зависит от их психотропной активности [9]. Высказывается предположение, что активность этих препаратов связана с модуляцией активности серотонинергических нейронов в ЦНС и с антагонизмом в отношении серотониновых рецепторов типа 5-НТ2 [4, 10, 14]. Это предположение основано на результатах экспериментальных и клинических исследований, свидетельствующих о повышенной чувствительности серотониновых рецепторов типа 5-НТ2 и
сниженном уровне серотонина в ЦНС в межприступном периоде болезни [3, 6, 7, 10], а также на данных о наличии у наиболее эффективных для профилактики антимигренозных средств антагонистических свойств в отношении 5-НТ2-рецепторов (метисергид, бета-блокаторы, некоторые антидепрессанты и блокаторы кальциевых каналов) [4]. Насколько важна для механизма антимигренозного действия антидепрессантов их способность модулировать активность норадренергической нейромедиаторной системы, неизвестно. При этом имеются убедительные данные об участии указанной моноаминергической системы в патогенезе мигрени [6, 7, 13, 15], а ряд эффективных антимигренозных препаратов обладает антиадренергическими свойствами (бета-адреноблокаторы, дигидроэрготамин, клонидин) [4, 10, 16].
Целью настоящего клинического исследования явилось сравнительное изучение антимигренозной активности антидепрессантов, избирательно модулирующих активность серотонинергической (флуоксетин) и норадренергической (мапротилин) нейромедиаторных систем, и амитриптилина, влияющего на обратный захват обоих нейромедиаторов, а также блокирующего серотониновые 5-
НТ 2-рецепторы.
Обследовали 60 пациентов, страдающих мигренью без ауры (табл. 1). Диагноз мигрени был установлен на основании диагностических критериев, предложенных Международным обществом по проблемам головной боли (IHS) [5]. Из сопутствующих заболеваний у 28 больных была эпизодическая и у 6 - хроническая головная боль напряжения, у 2 - лекарственная (абузусная) головная боль. Для выявления депрессии применяли шкалу Гамильтона. У 12 пациентов диагностирована депрессия легкой степени выраженности (7-14 баллов). С целью оценки эффективности проводившегося лечения мигрени использовали ежедневно заполняемый пациентом дневник с описанием типа головной боли, указанием частоты приступов, их тяжести, продолжительности, степени нарушения общего самочувствия и работоспособности, сопутствующих вегетативных проявлений (тошнота, свето-, звукобоязнь), количества принятых анальгетиков, переносимости лечения. Положительным результатом лечения считали уменьшение частоты приступов мигрени на 50% и более от исходной [8]. Для оценки влияния лечения на качество жизни применяли опросник качества жизни пациентов, страдающих мигренью.
| Таблица 1. Характеристика пациентов, принявших участие в исследовании
|
| Kритерий |
Амитриптилин |
Флуоксетин |
Мапротилин |
| Пол: |
| женщины |
18 |
19 |
20 |
| мужчины |
2 |
1 |
0 |
| Возраст, годы |
35,4(23-48) |
36,5(21-57) |
35,5(26-55) |
| Длительность болезни,годы |
15 (10-30) |
19(8-35) |
17(7-33) |
| Число пациентов с депрессией |
4 |
5 |
3 |
| Индекс качества жизни,баллы |
41,3 (35-56) |
40,9(36-58) |
38,6(29-52) |
|
| Примечание. Здесь и в табл. 2 приведены средние значения показателей, в скобках - диапазон колебаний. |
Методом случайной выборки пациентов разделили на три равные группы (по 20 человек): принимавших амитриптилин (12,5-25-50 мг 1 раз в сутки), флуоксетин (10-20 мг/сут также однократно) и мапротилин (10-25 мг/сут однократно). Использовали схему простого слепого исследования. При хорошей переносимости дозу препаратов увеличивали каждые 2 нед. Продолжительность лечения составила 12 нед. Контрольные исследования и коррекцию лечения проводили каждые 4 нед. Для купирования приступа применяли аспирин, парацетамол, индометацин и при необходимости их комбинации с метоклопрамидом (10 мг внутрь или 20 мг ректально). При тяжелых приступах ряд пациентов иногда использовали дигидроэрготамин (дигидергот - назальный спрей, "Novartis") и агонист 5-НТ1D-рецепторов золмитриптан (зомиг, "Zeneca").
Статистический анализ был выполнен с помощью непараметрического критерия Вилкоксона.
Полный курс лечения закончили 46 пациентов - 14 (70%) принимавших амитриптилин, 16 (80%) принимавших флуоксетин и 16 (80%) принимавших мапротилин. Выбыли из исследования 14 пациентов: 9 из-за побочных эффектов (4 из них принимали амитриптилин, 2 - флуоксетин, 3 - мапротилин) и 5 пациентов по причинам, не связанным с приемом антидепрессантов.
Только амитриптилин и флуоксетин достоверно снижали среднюю частоту приступов мигрени по сравнению с исходным периодом (табл. 2). Препараты достоверно уменьшали интенсивность головной боли и связанные с ней ограничения повседневной активности. Об уменьшении длительности приступа сообщили лишь пациенты, принимавшие амитриптилин. Уменьшение употребления препаратов для купирования приступа отмечено во всех трех группах. Снижение количества приступов на 50% и более по сравнению с исходным периодом установлено у 71% пациентов, принимавших амитриптилин, у 56% принимавших флуоксетин и у 38% - мапротилин (рис. 1). Курс проведенного лечения положительно отразился на качестве жизни пациентов, особенно в группах пациентов, принимавших амитриптилин и флуоксетин (рис. 2). Показатели шкалы депрессии Гамильтона нормализовались у всех 12 пациентов, причем быстрее всего у принимавших мапротилин (в среднем через 4-8 нед). Антидепрессанты в исследованных дозах уменьшали частоту и интенсивность сопутствующих головных болей напряжения, однако в связи с небольшим числом пациентов с данной патологией достоверных различий с исходным периодом получено не было.
| Таблица 2. Сравнительная оценка клинической эффективности антидепрессантов при профилактическом лечении мигрени |
| Показатель |
Амитриптилин |
Флуоксетин |
Мапротилин |
| I |
II |
p |
I |
II |
p |
I |
II |
p |
| Kоличество приступов за 4 нед |
6,9(3-10) |
3,8(1-5) |
0,001 |
6,2 (3-9) |
4,6 (1-8) |
0,05 |
6,5(3-8) |
5,4(2-7) |
Н.д. |
| Тяжесть приступа,баллы |
2,8(2-3) |
1,4(1-3) |
0,001 |
2,9(2-3) |
1,6(1-3) |
0,05 |
2,7 (2-3) |
1,6 (1-3) |
0,05 |
| Степень нарушения дееспособности, баллы |
2,2(1-3) |
1,5(0-2) |
0,05 |
2,4 (1-3) |
1,4(0-2) |
0,05 |
2,5(1-3) |
1,5(0-2) |
0,05 |
| Длительность приступа,баллы |
2,5(1-3) |
1,35(1-3) |
0,05 |
2,65(1-3) |
2,45(1-3) |
Н.д. |
2,55(1-3) |
2,2(1-3) |
Н.д. |
| Примечание. Н.д. - недостоверные различия. |
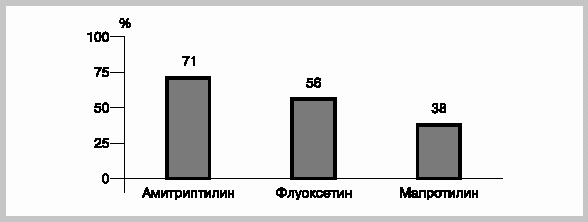 |
| Рис. 1. Количество пациентов, у которых число приступов мигрени уменьшилось более чем на 50% по сравнению с исходным. |
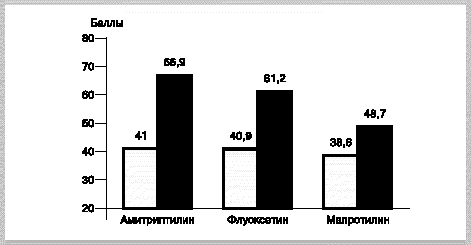 |
| Рис. 2. Динамика индекса качества жизни пациентов с мигренью после 12-недельного курса лечения антидепрессантами. |
| Светлые столбцы - до, темные - после лечения. |
Подавляющее большинство пациентов хорошо перенесли 12-недельный курс лечения. Предъявлявшиеся жалобы не носили выраженного характера и не стали поводом для отмены препаратов. Большинство побочных эффектов возникали в начале лечения и самостоятельно исчезали через 2 нед. Пациенты отметили лучшую переносимость мапротилина и флуоксетина по сравнению с амитриптилином (табл. 3).
Результаты проведенного исследования свидетельствуют о том, что антидепрессанты амитриптилин, флуоксетин и мапротилин проявляли разную эффективность при лечении мигрени в межприступном периоде. Наибольшей она оказалась у амитриптилина - трициклического антидепрессанта со свойствами ингибитора обратного захвата серотонина, норадреналина и антагониста 5-НТ2-рецепторов. Он достоверно уменьшал как частоту приступов, так и их тяжесть и продолжительность, при этом увеличивался индекс качества жизни. Больных с положительным результатом лечения в этой группе было на 15% больше, чем в группе принимавших флуоксетин, и на 33% больше, чем у принимавших мапротилин.
Флуоксетин - селективный ингибитор обратного захвата серотонина - уступал по эффективности амитриптилину, но был эффективнее мапротилина. Он уменьшал частоту и тяжесть приступов, повышал качество жизни пациентов, но не влиял на продолжительность приступов. Количество пациентов, у которых частота приступов снизилась более чем на 50% и достоверно повысился уровень качества жизни, оказалось большим, чем в группе принимавших мапротилин, соответственно на 18 и 10%.
Мапротилин - ингибитор обратного захвата норадреналина - в нашем исследовании оказался наименее эффективным. Положительные результаты лечения зарегистрированы у 38% пациентов этой группы, что, по данным литературы, сравнимо с эффективностью плацебо [11].
| Таблица 3. Частота побочных эффектов |
| Побочный эффект |
Амитриптилин |
Флуоксетин |
Мапротилин |
| абс. |
% |
абс. |
% |
абс. |
% |
| Сухость во рту |
8 |
40 |
5 |
25 |
6 |
30 |
| Сонливость |
9 |
45 |
6 |
30 |
5 |
25 |
| Возбудимость |
0 |
|
1 |
5 |
3 |
15 |
| Головокружение |
1 |
5 |
0 |
|
2 |
10 |
| Мышечная слабость |
5 |
25 |
2 |
10 |
1 |
5 |
| Тремор |
0 |
|
1 |
5 |
4 |
20 |
| Kоличество выбывших из-за побочных эффектов |
4 |
20 |
2 |
10 |
3 |
15 |
Высокая эффективность амитриптилина дает основание предположить, что антагонизм в отношении 5-
НТ2-рецепторов и ингибирование нейронального обратного захвата серотонина являются важным компонентом в механизме действия антидепрессантов при мигрени. Низкая эффективность ингибитора обратного захвата норадреналина - мапротилина говорит о том, что активация норадренергической системы в ЦНС не имеет существенного значения для антимигренозной активности антидепрессантов и косвенно свидетельствует в пользу того, что снижение избыточной активации норадренергической системы в межприступном периоде мигрени является одним из возможных механизмов действия таких профилактических антимигренозных препаратов, как бета-адреноблокаторы, дигидроэрготамин, клонидин.
Журнал неврологии и психиатрии N 8-2000, стр.20-23
1. Карлов В.А. Терапия нервных болезней. М: Медицина 1987.
2. Шток В.Н. Головная боль. М: Медицина 1987.
3. Diener H.C., May A. New aspects of migrain pathophysiology: lessons learned from positron emission tomography. Curr Opin Neurol 1996; 9: 199-201.
4. Goadsby P.J. How do the currently used prophylactic agents work in migrain? Cephalalgia 1997; 17: 85-92.
5. Headache Classification Criteria of International Headache Society: classification of diagnostic criteria for headache disorders, cranial neuralgias and facial pain. Cephalagia 1988; 8: suppl 7: 1-96.
6. Limmroth V., Cutrer F.M., Moskowitz M.A. Neurotransmitters and neuropeptides in headache. Curr Opin Neurol 1996; 9: 206-210.
7. Maertens de Noordhout A., Wang W., Schoenen J. Clinical neurophys-iology and neurotransmitters. Cephalalgia 1995; 15: 301-309.
8. Massiou H., Tzourio C., Bousser M.G. Methodology of Treatment Trials For Migrain Prophylaxis. In: J. Olesen, P. Tfelt-Hansen (eds.). Headache Treatment: Trial Methodology and New Drugs. New York: Lippincott-Raven 1997; 6: 125-135.
9. Peatfield R.C., Fozard J.R., Rose F.C. Drug treatment of migrain. In: Rose F.C. (ed.). Handbook of Clinical Neurology. New York: Elsevier 1986; 4: 173-216.
10. Peroutka S.J. The pharmacology of current antimigrain drugs. Headache 1990; 30: 1 (Suppl).
11. Ramadan N.M., Schultz L.L., Gilkey S.J. Migrain prophylactic drugs: proof of efficacy, utilization and cost. Cephalalgia 1997; 17: 73-80. 12. Rasmussen B.K. Epidemiology of Headache in Europe. In: J. Olesen (ed.). Headache Classification and Epidemiology. New York: Raven Press 1994; 231-237.
13. Shafar J., Tallett E.R. Evaluation of clonidine in prophylaxis of migrain. Lancet 1972; 1: 403-410.
14. Silberstein S.D. Preventive treatment of migraine: an overview. Cephalalgia 1997; 17: 67-72.
15. Zagami A.S. Pathophysiology o migrain and tensiontype headache.
Curr Opin Neurol 1994; 7: 272-277.
16. Zaimis E., Hanington E. A possible pharmacological approach to migraine. Lancet 1969; 2: 298-300.
Написать комментарий
|

